Βραβείο «Σ.Παπασταμάτης» Παν/λήνιο Ιατρικό Συνέδριο, Αθήνα 2012
ΜΕΛΕΤΗ ΤΩΝ ΠΙΟ ΑΝΤΙΓΟΝΙΚΩΝ B ΛΕΜΦΟΚΥΤΤΑΡΙΚΩΝ ΕΠΙΤΟΠΩΝ ΤΟΥ ΠΝΕΥΜΟΝΙΟΚΟΚΚΟΥ ΓΙΑ ΤΗΝ ΑΝΑΠΤΥΞΗ ΝΕΩΝ ΕΜΒΟΛΙΩΝ
Λαγκούση Θεανώ1, Ρούτσιας Ιωάννης2, Τσακρής Αθανάσιος2, Θεοδωρίδου Μαρία1 , Σπούλου Βάνα1
1: Α’ Παιδιατρική Κλινική Πανεπιστημίου Αθηνών, Νοσοκομείο Παίδων «Η Αγία Σοφία», Τμήμα Λοιμώξεων «ΜΑΚΚΑ»
2: Εργαστήριο Μικροβιολογίας, Ιατρική Σχολή Πανεπιστημίου Αθηνών
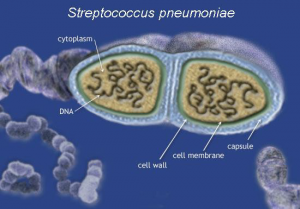
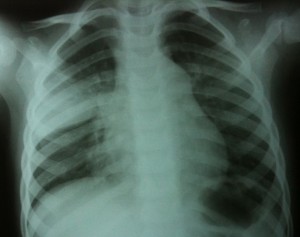
Ο πνευμονιόκοκκος (Εικόνα 1) ευθύνεται για σημαντικό ποσοστό θνητότητας και νοσηρότητας παγκοσμίως (> 1.5 εκατομμύρια θάνατοι), κυρίως σε παιδιά ηλικίας κάτω των 2 ετών, σε ηλικιωμένους (>65 ετών) και σε ανοσοκατασταλμένους ασθενείς [1]. Προκαλεί διεισδυτικές λοιμώξεις απειλητικές για τη ζωή όπως η μηνιγγίτιδα και η μικροβιαιμία αλλά και λιγότερο σοβαρές μη διεισδυτικές λοιμώξεις όπως η οξεία μέση ωτίτιδα (ΟΜΩ), η παραρρινοκολπίτιδα και η πνευμονία (Εικόνα 2).
Πρόκειται για ένα gram θετικό διπλόκοκκο της ομάδας των α-αιμολυτικών στρεπτόκοκκων που κατατάσσεται σε πάνω από 90 διαφορετικούς ορότυπους με βάση την πολυσακχαριδική του κάψα [2].
Το 23-δύναμο εμβόλιο (PPV23) περιέχει πολυσακχαριδικά αντιγόνα για 23 διαφορετικούς ορότυπους και συστήνεται σε παιδιά ηλικίας άνω των 2 ετών και στους ηλικιωμένους [3]. Το PPV23 προσφέρει προστασία μέσω της παραγωγής οψωνοφαγοκυτταρικών αντισωμάτων. Ωστόσο, επειδή η ανοσιακή απόκριση είναι θυμοανεξάρτητη, δεν εγκαθίσταται ανοσολογική μνήμη, με αποτέλεσμα να απαιτούνται επαναλαμβανόμενοι εμβολιασμοί, γεγονός που έχει συσχετιστεί μακροπρόθεσμα με ανεπαρκή ανοσολογική απάντηση (φαινόμενο υποαπαντητικότητας, hyporesponsivenes) [4].
Το πρώτο 7-δύναμο συζευγμένο πνευμονιοκοκκικό εμβόλιο (PCV7) περιλαμβάνει καθαρούς πολυσακχαρίτες για 7 ορότυπους συζευγμένους με μία διφθεριδική τοξίνη γνωστή ως CRM197 (Prevenar, Pfizer). Το PCV7 είναι πιο ανοσογονικό στις μικρές ηλικίες και στους ανοσοκατασταλμένους ασθενείς και εγκαθιστά ανοσολογική μνήμη μέσω της θυμοεξαρτώμενης ανοσιακής απάντησης [5]. Το PCV7, όπως και το PPV23, προστατεύει ειδικά έναντι της λοίμωξης από τους ορότυπους που περιλαμβάνονται σε αυτό, ενώ προσφέρει και συλλογική προστασία σε άνοσους πληθυσμούς (herd immunity). Ωστόσο, η διαφορετική επιδημιολογία της πνευμονιοκοκκικής λοίμωξης μεταξύ αναπτυγμένων και αναπτυσσόμενων χωρών, έχει ως αποτέλεσμα το PCV7 να καλύπτει μόνο το 1/4 της πνευμονιοκοκκικής λοίμωξης σε κάποιες αναπτυσσόμενες χώρες [6]. Επιπλέον, μετά την ευρεία χρήση του PCV7 παρατηρήθηκε το φαινόμενο της αντικατάστασης των ορότυπων του εμβολίου με άλλους που δεν περιλαμβάνονται σε αυτό, με κυριότερο τον ορότυπο 19Α (replacement) [7]. Παρά την κυκλοφορία δύο ευρύτερης κάλυψης πνευμονιοκοκκικών εμβολίων, του 10-δύναμου συζευγμένου με την πρωτεΐνη D του Αιμόφιλου της Ινφλουέντζας (NTHi) (PCV10) (Synflorix, GSK) και του 13-δύναμου-CRM197 (Prevenar 13, Pfizer), η παρεχόμενη προστασία παραμένει περιορισμένη σε συγκεκριμένο αριθμό ορότυπων, ενώ το κόστος παραγωγής δεν επιτρέπει την ευρεία χρήση τους στις αναπτυσσόμενες χώρες.
Σύντομα, το ενδιαφέρον στράφηκε στις πρωτεΐνες που βρίσκονται στην επιφάνεια του πνευμονιόκοκκου, και παίζουν σημαντικό ρόλο στην παθογονικότητά του. Πειραματικά μοντέλα ζώων έχουν επιβεβαιώσει την ανοσογονικότητα και την προστατευτική ικανότητα πολλών από αυτές τις πρωτεΐνες τόσο στη διεισδυτική πνευμονιοκοκκική λοίμωξη όσο και στον αποικισμό του ρινοφάρυγγα, το στάδιο που προηγείται της φυσικής λοίμωξης [8]. Μάλιστα, κάποιες από αυτές έχουν δοκιμαστεί σε ενήλικες με αρκετά ενθαρρυντικά αποτελέσματα [9]. Ωστόσο, η μεγάλη ποικιλομορφία των πρωτεϊνών αυτών αλλά και η αδυναμία τους να προάγουν την παραγωγή αποτελεσματικών αντισωμάτων τις καθιστά ακατάλληλες για την κατασκευή εμβολίων [10].
Πρόσφατα, νέες μέθοδοι αναπτύχθηκαν με σκοπό τον προσδιορισμό νέων αντιγόνων του πνευμονιόκοκκου. Η αντίστροφη ανοσολογία (reverse vaccinology) μελετά το πλήρες γονιδίωμα του πνευμονιόκοκκου και προβλέπει με τεχνικές βιοπληροφορικής τα αντιγόνα που εκφράζονται στη επιφάνειά του και επομένως αποτελούν δυνητικά στόχους της αντισωματικής απάντησης του ξενιστή [11].
Την τελευταία δεκαετία, μία άλλη μέθοδος άρχισε να κερδίζει έδαφος στηριζόμενη στην ανίχνευση αντιγόνων τα οποία αναγνωρίζονται από ασθενείς με διεισδυτική πνευμονιοκοκκική λοίμωξη (antigenomics technology) [12]. Η μέθοδος αυτή εξασφαλίζει τον προσδιορισμό των πιο αντιγονικών Β λεμφοκυτταρικών επιτόπων κατά τη φυσική λοίμωξη, μιας και ο άνθρωπος είναι ο μόνος φυσικός ξενιστής του πνευμονιόκοκκου. Προηγούμενη μελέτη στηριζόμενη στη μέθοδο αυτή προσδιόρισε 9 κυρίαρχους αντιγονικούς καθοριστές που εντοπίζονται σε τμήματα πρωτεϊνών του πνευμονιόκοκκου και ενέχονται στην αναγνώριση του μικροβίου από το ανοσολογικό σύστημα του ξενιστή [13]. Οι πρωτεΐνες αυτές είναι οι histidine-triad proteins (PhtE, PhtD), pneumococcal surface protein A (PspA), choline-binding protein D (CbpD), zinc metalloproteinase B (ZmpB) και pneumococcal adherence and virulence factor B (PavB) που κωδικοποιείται από το ORF spr0075 (Spr0075). Ωστόσο, το μεγάλο μέγεθος των αντιγονικών αυτών θραυσμάτων δεν επιτρέπει τη συνθετική παρασκευή τους στη μορφή πεπτιδίων.
Σκοπός της παρούσας μελέτης ήταν ο προσδιορισμός των κυριότερων αντιγονικών Β λεμφοκυτταρικών επιτόπων, που περιέχονται στις αντιγονικές περιοχές που ανιχνεύθηκαν στην προηγούμενη αυτή μελέτη [13], με σκοπό τη χρήση τους σε διαγνωστικές και προληπτικές εφαρμογές.
Με τη μέθοδο της πολλαπλής χαρτογράφησης με εφιππευόμενα πεπτίδια (multipin epitope mapping technology), έγινε λεπτομερής προσδιορισμός σε επίπεδο αμινοξέος των κυριότερων αντιγονικών Β λεμφοκυτταρικών επιτόπων. Για το σκοπό αυτό, χρησιμοποιήθηκαν οροί από ασθενείς με διεισδυτική πνευμονιοκοκκική λοίμωξη οι οποίοι αναγνώρισαν σε βαθμό στατιστικά σημαντικό 10 Β λεμφοκυτταρικούς επιτόπους. Μάλιστα, με τη βοήθεια της βιολογικής βάσης δεδομένων (ΒΒΔ) Uniprot διαπιστώθηκε ότι 4 από τους 10 αυτούς τους επιτόπους επαναλαμβάνονται μέσα στην πατρική πρωτεΐνη, γεγονός που αυξάνει δυνητικά τη συνάφεια αλληλεπίδρασης τους με τα ειδικά πνευμονιοκοκκικά αντισώματα (avidity). Επιπλέον, σύγκριση της αμινοξικής αλληλουχίας των 10 κυρίαρχων αντιγονικών Β λεμφοκυτταρικών επιτόπων στην ίδια ΒΒΔ αποκάλυψε ότι οι επίτοποι αυτοί παρουσιάζουν μεγάλη ομολογία μεταξύ των διαφορετικών ορότυπων (95-100%), ενώ η ομολογία με άλλους στρεπτοκόκκους και βακτήρια φτάνει μόλις το 80-85%. Στη συνέχεια, τα 10 επιλεγμένα πεπτίδια συντέθηκαν εκ νέου σε διαλυτή μορφή και επιβεβαιώθηκε η αντιγονικότητά τους έναντι μεγάλου αριθμού ασθενών με διεισδυτική πνευμονιοκοκκική λοίμωξη, με τη βοήθεια ανοσοενζυμικής τεχνικής στερεάς φάσης που διαμορφώθηκε κατάλληλα (ELISA).
Συμπερασματικά, ο προσδιορισμός των πιο αντιγονικών Β λεμφοκυτταρικών επιτόπων των πνευμονιοκοκκικών πρωτεϊνών ενθαρρύνει την περαιτέρω μελέτη τους για τη χρησιμοποίησή τους στο σχεδιασμό διαγνωστικών ανοσοενζυμικών μεθόδων αυξημένης ευαισθησίας και ειδικότητας για τη διεισδυτική πνευμονιοκοκκική λοίμωξη. Επιπλέον, η ικανότητά των επιτόπων αυτών να παράγουν οψωνοφαγοκυτταρικά αντισώματα, αν αποδειχθεί, θα επιτρέψει τη συμμετοχή τους στο σχεδιασμό εμβολίου που θα παρέχει ευρεία προστασία έναντι μεγάλου αριθμού παθογόνων πνευμονιοκοκκικών ορότυπων.
ΒΙΒΛΙΟΓΡΑΦΙΑ
- Rudan I, Boschi-Pinto C, Biloglav Z, Mulholland K, Campbell H. Epidemiology and etiology of childhood pneumonia. Bull World Health Organ 2008, 86:408-16.
- Bentley SD, Aanensen DM, Mavroidi A, Saunders D, Rabbinowitsch E, Collins M et al. Genetic analysis of the capsular biosynthetic locus from all 90 pneumococcal serotypes. PLoS Genet 2006, 2(3):e31.
- Mangtani P, Cutts F, Hall AJ. Efficacy of polysaccharide pneumococcal vaccine in adults in more developed countries: the state of the evidence. Lancet Infect Dis 2003, 3:71 – 78.
- Russell FM, Carapetis JR, Balloch A, Licciardi PV, Jenney AW, Tikoduadua L et al. Hyporesponsiveness to re-challenge dose following pneumococcal polysaccharide vaccine at 12 months of age, a randomized controlled trial. Vaccine 2010, 28:3341-9.
- Bogaert D, Hermans PW, Adrian PV, Rümke HC, de Groot R. Pneumococcal vaccines: an update on current strategies. Vaccine 2004, 22:2209-20.
- Van Dam JE, Fleer A, Snippe H. Immunogenicity and immunochemistry of Streptococcus pneumoniae capsular polysaccharides. Antonie Van Leeuwenhoek. 1990;58:1-47.
- Herz AM, Greenhow TL, Alcantara J, Hansen J, Baxter RP, Black SB et al. Changing epidemiology of outpatient bacteremia in 3- to 36-month-old children after the introduction of the heptavalent-conjugated pneumococcal vaccine. Pediatr Infect Dis J 2006, 25:293-300.
- Tai SS, Streptococcus pneumoniae protein vaccine candidates: properties, activities and animal studies. Crit Rev Microbiol. 2006;32:139-53
- Kamtchoua T, Bologa M, Hopfer R, Neveu D, Hu B, Sheng X et al. Safety and immunogenicity of the pneumococcal pneumolysin derivative PlyD1 in a single-antigen protein vaccine candidate in adults. Vaccine. 2012 Nov 12. pii: S0264-410X(12)01598-8. doi: 10.1016/j.vaccine.2012.11.005.
10. Overweg K et al. Differential protein expression in phenotypic variants of Streptococcus pneumoniae. Infection and Immunity, 2000, 68:4604–4610.
11. Barocchi MA, Censini S, Rappuoli R. Vaccines in the era of genomics: the pneumococcal challenge. Vaccine 2007, 25:2963-73.
12. Giefing C, Nagy E, Von Gabain A. The antigenome: from protein subunit vaccines to antibody treatments of bacterial infections? Adv Exp Med Biol 2009;655:90-117.
13. Beghetto E, Gargano N, Ricci S, Garufi G, Peppoloni S, Montagnani F et al. Discovery of novel Streptococcus pneumoniae antigens by screening a whole-genome lambda-display library. FEMS Microbiol Lett 2006, 262:14-21.