Εισαγωγή:
Η παχυσαρκία αποτελεί ένα σοβαρότατο και ταχέως εξελισσόμενο πρόβλημα υγείας. Σύμφωνα με τον Παγκόσμιο Οργανισμό Υγείας, μέχρι το 2008 ο αριθμός των υπέρβαρων ατόμων άνω των 20 ετών έφτανε τα 1.4 δισεκατομμύρια, ενώ 500 εκατομμύρια ήταν παχύσαρκα, βάσει του εκτιμώμενου Δείκτη Μάζας Σώματος (BMI). Ανησυχητικό είναι και το ποσοστό των ανήλικων υπέρβαρων ατόμων, το οποίο προσεγγίζει το 7-10% του πληθυσμού και αναμένεται να διπλασιαστεί μέχρι το 2025, ενώ ταυτόχρονα, υπάρχει μεγάλη πιθανότητα να διατηρηθεί το αυξημένο σωματικό βάρος και στην ενήλικη ζωή.1 Η παχυσαρκία συνδέεται με αυξημένη συνολική θνητότητα. Το 2010 εκτιμήθηκε ότι η παχυσαρκία ήταν η βαθύτερη αιτία για 3.4 εκατομμύρια θανάτους παγκοσμίως, λόγω των συννοσηροτήτων που τη συνοδεύουν. Συγκεκριμένα, η παχυσαρκία σχετίζεται με αυξημένο κίνδυνο υπέρτασης, δυσλιπιδαιμίας, αντίστασης στην ινσουλίνη και ανάπτυξης διαβήτη τύπου 2, εμφράγματος του μυοκαρδίου, ισχαιμικών αγγειακών εγκεφαλικών επεισοδίων, αλλά και με αυξημένη φλεγμονή, υπνική άπνοια, διαταραχές του συμπαθητικού συστήματος, συγκεκριμένα είδη καρκίνων και οστεοαρθρίτιδα.2 Είναι αδιαμφισβήτητο λοιπόν, ότι η παχυσαρκία υποβαθμίζει την ποιότητα ζωής, ενώ ταυτόχρονα ενέχει μεγάλο υγειονομικό κόστος.
Η πρόληψη και αντιμετώπιση της παχυσαρκίας, λοιπόν, γίνεται επιτακτική ανάγκη στις μέρες μας, δεδομένης της ραγδαίας εξάπλωσης της νόσου σε ανεπτυγμένες και αναπτυσσόμενες χώρες. Το πρώτο βήμα αποτελούσε πάντα η παρέμβαση στον τρόπο ζωής με την εφαρμογή υποθερμιδικής δίαιτας και οδηγίες για την αύξηση της σωματικής δραστηριότητας. Η κλινική εμπειρία, όμως, έχει δείξει πως αυτού του είδους η παρέμβαση δεν έχει συχνά αξιόλογο και το κυριότερο διατηρήσιμο αποτέλεσμα. Στο άλλο άκρο των θεραπευτικών παρεμβάσεων υπάρχει και διαρκώς εξελίσσεται η βαριατρική χειρουργική, η οποία εξασφαλίζει όλο και καλύτερα αποτελέσματα. Ενέχει όμως τον κίνδυνο περιεγχειρητικής νοσηρότητας και θνητότητας και χειρουργικών επιπλοκών, ο δε τρόπος ζωής των ασθενών αλλάζει οριστικά. Για το λόγο αυτό επιφυλάσσεται στις περιπτώσεις νοσογόνου παχυσαρκίας.3 Καταδεινύεται κατόπιν τούτων η σημασία ενίσχυσης της υγιεινοδιαιτητικής παρέμβασης με φαρμακευτικές ουσίες, οι οποίες όμως θα πρέπει να χαρακτηρίζονται από ικανοποιητική αποτελεσματικότητα, διατηρησιμότητα του αποτελέσματος και όσο το δυνατόν λιγότερες ανεπιθύμητες ενέργειες.
Φαρμακευτική αντιμετώπιση της παχυσαρκίας
Παρελθόν:
Οι πρώτες σοβαρές προσπάθειες για τη φαρμακευτική απώλεια βάρους έγιναν από τον Baron το 1893, ο οποίος χορήγησε θυρεοειδική ορμόνη, ορμώμενος από το κλινικό αποτέλεσμα στο σωματικό βάρος ασθενών με υποθυρεοειδισμό και μυξοίδημα. Στη συνέχεια, εμφανίστηκε η δινιτροφαινόλη (1933), η οποία είχε μεν ευεργετικό αποτέλεσμα στο βάρος, όμως προκαλούσε νευροπάθεια, καταρράκτη και συνδέθηκε με θανάτους.5
Μετά τον Β΄ Παγκόσμιο Πόλεμο εμφανίστηκε στο προσκήνιο η αμφεταμίνη με τα παράγωγά της, κυριότερα των οποίων ήταν η δεσοξυεφεδρίνη, η φεντερμίνη και η διαιθυλπροπιόνη.6 Αυτά τα κεντρικώς δρώντα συμπαθητικομιμητικά έγιναν πολύ δημοφιλή στις δεκαετίες του ’50 και του ’60, όμως ο κίνδυνος εξάρτησης και ο αυξημένος κίνδυνος για υπέρταση και καρδιαγγειακά συμβάματα οδήγησαν στην απόσυρσή τους.5,6 Τη θέση τους δεν άργησαν να πάρουν η φαινφλουραμίνη (1963) και η δεξφαινφλουραμίνη (1985), οι οποίες δρουν σεροτονινεργικά καταστέλλοντας την πείνα. Τα φάρμακα αυτά ήταν γνωστό ότι μπορούσαν να προκαλέσουν πνευμονική υπέρταση, ωστόσο το όφελος από την απώλεια βάρους θεωρείτο ότι αντιστάθμιζε τον κίνδυνο. Τελικά, μελέτες ενοχοποίησαν τους συγκεκριμένους παράγοντες για βαλβιδοπάθειες, οδηγώντας στην απόσυρσή τους στη δεκαετία του ’90. Την ίδια εποχή δοκιμάστηκε και η συγχορήγηση της φαινφλουραμίνης μαζί με φεντερμίνη. Ο συνδυασμός (fen-phen) είχε εξαιρετικά αποτελέσματα στην απώλεια βάρους, όμως διαπιστώθηκε το 1997 ότι ο κίνδυνος ανάπτυξης βαλβιδοπάθειας άγγιζε το 30%, με αποτέλεσμα την απόσυρσή του.4,5
Στα τέλη της δεκαετίας του 1990 κυκλοφόρησε η σιβουτραμίνη, ένας αναστολέας επαναπρόσληψης νοραδρεναλίνης και σεροτονίνης, ο οποίος αρχικά αναπτύχθηκε ως αντικαταθλιπτικό φάρμακο. Διαπιστώθηκε ωστόσο ότι αυξάνει το αίσθημα κορεσμού και την περιφερική θερμογένεση, επιφέροντας απώλεια βάρους, με αποτέλεσμα να πάρει έγκριση το 1998 ως φάρμακο κατά της παχυσαρκίας5. Μετά την κυκλοφορία και την ευρεία χρήση της σιβουτραμίνης όμως, διαπιστώθηκαν ανεπιθύμητες ενέργειες από το συμπαθητικό νευρικό σύστημα, με σημαντικότερες την αύξηση της αρτηριακής πίεσης και της καρδιακής συχνότητας. Ζητήθηκε λοιπόν να διεξαχθεί μελέτη καρδιοαγγειακού κινδύνου για τη σιβουτραμίνη, μετά την κυκλοφορία της. Έτσι διεξήχθη η μελέτη SCOUT (Sibutramine Cardiovascular Outcomes Trial), στην οποία σημειώθηκε αυξημένος αριθμός μη θανατηφόρων οξέων εμφραγμάτων του μυοκαρδίου, αλλά και αγγειακών εγκεφαλικών επεισοδίων σε ασθενείς υψηλού κινδύνου που έπαιρναν σιβουτραμίνη, έναντι εικονικού φαρμάκου (placebo).4 Συνεπώς, το 2010 η σιβουτραμίνη εμπλούτισε τον κατάλογο των αποσυρμένων φαρμάκων για την παχυσαρκία.8
Στο πιο πρόσφατο παρελθόν, η εμφάνιση του rimonabant την δεκαετία του 2000 γέννησε νέες ελπίδες για την αντιμετώπιση της παχυσαρκίας. Ο συγκεκριμένος παράγοντας είναι ανταγωνιστής των CB1 υποδοχέων των ενδογενών κανναβινοειδών, ο οποίος μείωνε σημαντικά την πρόσληψη τροφής, μέσω της καταστολής του αισθήματος ανταμοιβής. Παράλληλα, εκτός από τους κεντρικούς, είχε επίδραση και στους περιφερικούς CB1 υποδοχείς, με αποτέλεσμα τη μείωση της λιπογένεσης και της ινσουλινοαντοχής, τη βελτίωση του λιπιδαιμικού προφίλ και την αύξηση των συγκεντρώσεων αδιπονεκτίνης και των περιφερικών σημάτων κορεσμού.5,9 Πραγματοποιήθηκαν τέσσερις μεγάλες τυχαιοποιημένες κλινικές μελέτες, οι οποίες έδειξαν σημαντική ανωτερότητα του rimonabant έναντι του placebo όσον αφορά την απώλεια βάρους. Το 2006 το φάρμακο πήρε έγκριση κυκλοφορίας, όμως, μετά την ευρεία χρήση του, διαπιστώθηκαν ψυχιατρικές ανεπιθύμητες ενέργειες, όπως άγχος, κατάθλιψη και κυρίως αυτοκτονικός ιδεασμός. Η τελευταία αποτέλεσε και τον λόγο για τον οποίο το 2008 το rimonabant αποσύρθηκε οριστικά.5
Παρόν:
Επί του παρόντος, το μόνο εγκεκριμένο φάρμακο κατά της παχυσαρκίας στην Ευρώπη είναι η ορλιστάτη. Ο παράγοντας αυτός αναστέλλει εν μέρει τη δράση των παγκρεατικών και εντερικών λιπασών, με αποτέλεσμα να μειώνεται η απορρόφηση του προσλαμβανόμενου με την τροφή λίπους κατά περίπου 30%.7 Η αποτελεσματικότητα του φαρμάκου φάνηκε σε αρκετές κλινικές μελέτες, κυριότερη των οποίων ήταν η XENDOS, μια διπλή-τυφλή τυχαιοποιημένη κλινική μελέτη με 3305 συμμετέχοντες. Η μελέτη έδειξε μέση απώλεια βάρους 5.8 kg έναντι 3.0 kg με το εικονικό φάρμακο. Ταυτόχρονα, η περαιτέρω απώλεια βάρους μείωσε τον κίνδυνο εμφάνισης σακχαρώδους διαβήτη τύπου 2 κατά 37.3% στο σύνολο των συμμετεχόντων και κατά 45% σε ασθενείς με διαταραγμένη ανοχή στη γλυκόζη (Σχήμα 1). Ακόμη, μείωσε τα επίπεδα της LDL χοληστερόλης, αλλά και της αρτηριακής πίεσης.10 Η ένδειξη χορήγησης της ορλιστάτης είναι σε ασθενείς με Δείκτη Μάζας Σώματος μεγαλύτερο από 30 kg/m2 χωρίς συνοδούς παράγοντες καρδιοαγγειακού κινδύνου, ή μεγαλύτερο από 27 kg/m2 και τουλάχιστον έναν παράγοντα κινδύνου, αφού έχει αποτύχει η παρέμβαση στον τρόπο ζωής, πάντα σε συνδυασμό με υποθερμιδική δίαιτα και άσκηση. Οι ανεπιθύμητες ενέργειες της ορλιστάτης περιορίζονται στο γαστρεντερικό σύστημα, με πιο συνήθεις την ήπια στεατόρροια, τον αυξημένο αριθμό κενώσεων, τη δυσπεψία και το μετεωρισμό. Διχογνωμία υπάρχει για το αν η ορλιστάτη προκαλεί δυσαπορρόφηση των λιποδιαλυτών βιταμινών και άλλων συγχορηγούμενων φαρμάκων, ωστόσο αυτή η ανησυχία δεν έχει επιβεβαιωθεί.3,5,10
Νέα φάρμακα:
Στην Αμερική έχουν εμφανισθεί κάποιες νέες προοπτικές στην φαρμακευτική παρέμβαση κατά της παχυσαρκίας και υπόσχονται θετικά αποτελέσματα, ωστόσο στην Ευρώπη επικρατεί σκεπτικισμός λόγω των ενδεχόμενων ανεπιθύμητων ενεργειών. Τα καινούρια φάρμακα στοχεύουν σε μονοπάτια του κεντρικού νευρικού συστήματος που είναι υπεύθυνα για το αίσθημα κορεσμού και τη ρύθμιση της όρεξης.6 Επίσης, επιχειρείται ο συνδυασμός διαφορετικών παραγόντων, ούτως ώστε να επιτευχθεί συνεργική δράση με λιγότερες ανεπιθύμητες ενέργειες.3,8
Βουπροπιόνη/Ναλτρεξόνη
Ο συνδυασμός βουπροπιόνης/ναλτρεξόνης πήρε πρόσφατα έγκριση κυκλοφορίας από τον Αμερικανικό Οργανισμό Φαρμάκων (FDA).8 Η καινοτομία του συγκεκριμένου συνδυαστικού παράγοντα έγκειται στον τρόπο δράσης του στο κεντρικό νευρικό σύστημα. Έχει βρεθεί ότι η διατροφική συμπεριφορά ρυθμίζεται από συγκεκριμένες περιοχές του εγκεφάλου, ιδιαίτερα τον τοξοειδή πυρήνα του υποθαλάμου, απ’ όπου σηματοδοτούνται σήματα σε ανώτερα κέντρα. Οι παχύσαρκοι παρουσιάζουν πιθανώς διαταραγμένη ισορροπία της δραστηριότητας των νευρώνων που εμπλέκονται στην πρόσληψη τροφής. 4,8,11 Στον τοξοειδή πυρήνα ευρίσκονται δύο κυρίως πληθυσμοί νευρώνων, εκείνοι που εκκρίνουν τα ανορεξιογόνα νευροπεπτίδια προοπιομελανοκορτίνη (POMC) και Cocaine and Amphetamine Regulated Transcript (CART), και άλλοι που εκκρίνουν τα ορεξιογόνα σήματα νευροπεπτίδιo Υ (NPY) και Agouti-related Protein (AGRP). Συγκεκριμένα, το σύστημα των μελανοκορτινών, που εδράζεται μεταξύ άλλων περιοχών του ΚΝΣ και στον υποθάλαμο, παίζει σημαντικό ρόλο στους ομοιοστατικούς μηχανισμούς που αφορούν το ισοζύγιο της ενέργειας. Η έκκριση της POMC οδηγεί τελικά στην παραγωγή της α-MSH (α-Melanin Stimulating Hormone) που έχει ισχυρή ανορεξιογόνο επίδραση. Παράλληλα όμως, το πολύπλοκο αυτό σύστημα διαθέτει μηχανισμούς αρνητικής ανατροφοδότησης. Έτσι, η β-ενδορφίνη που είναι επίσης προϊόν της POMC, συνδέεται με τους μ-υποδοχείς οπιοειδών, ενεργοποιώντας έναν μοριακό καταρράκτη που καταλήγει στην αδρανοποίηση των POMC κυττάρων. Εκτός από αυτό το μονοπάτι, έχει επίσης μελετηθεί και το σύστημα της ανταμοιβής που εδρεύει στο μεσεγκέφαλο, αλλά επηρεάζει και επηρεάζεται από πολλές περιοχές του εγκεφάλου. Σε αυτήν την περιοχή, ρυθμιστικό ρόλο έχουν η ντοπαμίνη και τα οπιοειδή, ευωδώντας την πρόσληψη τροφής. Ωστόσο, οι νευρώνες της περιοχής έχουν την ικανότητα να προσαρμόζονται σε χρόνια ερεθίσματα, με αποτέλεσμα την απαίτηση μεγαλύτερων ποσών τροφής, ώστε να προκύψει αίσθημα ανταμοιβής. Η διαταραχή αυτή παρατηρείται συχνά στους παχύσαρκους.4,11
Η βουπροπιόνη είναι ένας μη εκλεκτικός αναστολέας επαναπρόσληψης νορεπινεφρίνης και ντοπαμίνης και χρησιμοποιείται ως τώρα για την αντιμετώπιση της κατάθλιψης, της εποχιακής κατάθλιψης και για τη διευκόλυνση της διακοπής του καπνίσματος. Βρέθηκε πως η βουπροπιόνη διεγείρει τους POMC νευρώνες, προκαλώντας ανορεξιογόνο επίδραση, η οποία επιπλέον ενισχύεται από τις ντοπαμινεργικές και νοραδρενεργικές της ιδιότητες. Ωστόσο, η απώλεια βάρους που μπορεί να παράγει μόνη της φάνηκε ότι δεν ήταν σημαντική. Από την άλλη μεριά, η ναλτρεξόνη είναι ένας ανταγωνιστής των υποδοχέων των οπιοειδών, η οποία χρησιμοποιείται στην απεξάρτηση από την κατάχρηση οινοπνεύματος και οπιοειδών. Έχει διττή δράση στα συστήματα της πρόσληψης τροφής. Αναστέλλει τους μ- υποδοχείς των οπιοειδών, μειώνοντας έτσι την αρνητική ανατροφοδότηση στην έκκριση α-MSH από τους POMC νευρώνες. Ταυτόχρονα, δρα ανασταλτικά στους υποδοχείς του συστήματος της ανταμοιβής, αυξάνοντας έτσι την ανορεξιογόνο επίδραση του συνδυασμού της με τη βουπροπιόνη. Χορηγούμενη μόνη της στις συνήθεις δόσεις της απεξάρτησης δεν έδειξε σημαντική επίδραση στο βάρος, ενώ χορηγούμενη σε μεγαλύτερη δόση είναι ηπατοτοξική. Έτσι, δοκιμάστηκε η συγχορήγηση των δύο παραγόντων με το εξής σκεπτικό: η χορήγηση βουπροπιόνης διεγείρει τα POMC κύτταρα, αλλά ταυτόχρονα η ναλτρεξόνη εμπλέκεται στον μηχανισμό αρνητικής ανατροφοδότησης των κυττάρων αυτών, αδρανοποιώντας τον, προσφέροντας έτσι αθροιστικό αποτέλεσμα. (Εικόνα 1)4,11
Σειρά κλινικών μελετών εξήτασε την αποτελεσματικότητα του συνδυασμού βουπροπιόνης/ναλτρεξόνης σε άτομα με ή χωρίς διαβήτη, αποδεικνύοντας τη σημαντική του επίδραση στο σωματικό βάρος (COR-I, COR-II, COR-III, COR-BMOD, COR-D) (Σχήμα 2).4,11,12 Στις μελέτες φάσης ΙΙΙ διαπιστώθηκε μικρή αύξηση της αρτηριακής πίεσης και της καρδιακής συχνότητας. Για το λόγο αυτό, ο FDA ζήτησε την διεξαγωγή μελέτης καρδιοαγγειακού κινδύνου, προτού δώσει την τελική έγκριση κυκλοφορίας. Το Σεπτέμβριο του 2014 ο συνδυασμός έλαβε έγκριση για κυκλοφορία στις ΗΠΑ και το Δεκέμβριο του ιδίου έτους στην Ευρώπη.5,8 Οι ανεπιθύμητες ενέργειες του φαρμάκου είναι κυρίως η ναυτία, οι έμετοι, η δυσκοιλιότητα, ο κοιλιακός πόνος, η ημικρανία και η αϋπνία. Υπάρχουν επιπλέον ορισμένες ανησυχίες για ψυχιατρικές ανεπιθύμητες ενέργειες, κυρίως αυτοκτονικό ιδεασμό.4,5,11
Φεντερμίνη/Τοπιραμάτη
Ένας άλλος συνδυασμός που επίσης κυκλοφόρησε προσφάτως στις ΗΠΑ είναι αυτός φεντερμίνης και τοπιραμάτης. Η φεντερμίνη είναι άτυπο ανάλογο της αμφεταμίνης, με ανορεξιογόνο δράση, η οποία, στο συνδυασμό, χορηγείται σε μικρότερη δόση από τη συνηθισμένη, που είχε αποδειχθεί δυνητικά επιβλαβής στο παρελθόν.3,13 Δρα κυρίως νοραδρενεργικά, επάγοντας ανορεξία (και πιθανώς αυξάνοντας τη θερμογένεση). Η τοπιραμάτη είναι ένα αντιεπιληπτικό φάρμακο, το οποίο, στο συνδυασμό, χορηγείται επίσης σε μικρότερη δόση από αυτή που συνηθίζεται για την επιληψία και επιπλέον σε μορφή βραδείας αποδέσμευσης. Ο μηχανισμός επίδρασης στην όρεξη δεν έχει πλήρως αποσαφηνιστεί, αλλά πιθανώς σχετίζεται με τη διέγερση των υποδοχέων του γ-αμινοβουτυρικού οξέος.13 Στις μεγάλες μελέτες EQUIP και CONQUER, καθώς και στην επέκταση της τελευταίας, τη μελέτη SEQUEL, εδείχθη η υπεροχή του συνδυασμού φεντερμίνης/τοπιραμάτης στην απώλεια βάρους έναντι του εικονικού φαρμάκου (σχήμα 3), ενώ ταυτόχρονα φάνηκε ότι σε μέση και υψηλή δόση, μείωνε τη συστολική και τη διαστολική αρτηριακή πίεση. Σε όλες τις χορηγούμενες δοσολογίες, όμως, αύξανε τον καρδιακό ρυθμό, ενώ τα δεδομένα για την καρδιοαγγειακή ασφάλεια δεν είναι επαρκή.13-17 Έτσι, ο συνδυασμός είναι εγκεκριμένος από το 2012 στην Αμερική υπό πολλούς περιορισμούς, ενώ στην Ευρώπη αναμένεται η διερεύνηση της καρδιοαγγειακής ασφάλειας για να συζητηθεί η έγκριση κυκλοφορίας, ενώ επιπλέον υπάρχουν ανησυχίες για πιθανές ψυχιατρικές και γνωσιακές διαταραχές, καθώς και για την πιθανότητα κατάχρησης.4 Εξάλλου, η τοπιραμάτη είναι τερατογόνος και γι αυτό υπάρχει αυστηρή αντένδειξη χορήγησης του φαρμάκου στην κύηση. Άλλες ανεπιθύμητες ενέργειες που έχουν σημειωθεί είναι η δυσκοιλιότητα, η ξηροστομία, το αίσθημα παλμών, παραισθησίες, διαταραχές της προσοχής, αλλοιώσεις της γεύσης, μεταβολική οξέωση, νεφρολιθίαση, αλωπεκία και υποκαλιαιμία.4,5
Λορκασερίνη
Ένας ακόμη κεντρικώς δρών παράγοντας κατά της παχυσαρκίας είναι η λορκασερίνη. Πρόκειται για έναν εκλεκτικό αγωνιστή των υποδοχέων 5-ΗΤ2c της σεροτονίνης, οι οποίοι βρίσκονται ως επί το πλείστον στον υποθάλαμο. Συνδεόμενη με τους υποδοχείς αυτούς, προκαλεί την παραγωγή α-MSH, η οποία επιδρά με ανορεξιογόνο τρόπο στο σύστημα των μελανοκορτινών.4,16 Η λορκασερίνη στερείται συγγένειας για τους σεροτονινεργικούς υποδοχείς που βρίσκονται στις βαλβίδες της καρδιάς, έτσι ώστε θεωρητικά να μην αναμένονται οι σοβαρές ανεπιθύμητες ενέργειες που αφορούσαν βαλβιδοπάθειες και αποτελούσαν πρόβλημα με προγενέστερους σεροτονινεργικούς αγωνιστές (π.χ. φαινφλουραμίνη).4 Η αποτελεσματικότητα της λορκασερίνης εδείχθη με δύο κυρίως μεγάλες κιλινκές μελέτες (BLOOM, BLOSSOM), όπου φάνηκε να έχει μέτρια επίδραση στην απώλεια βάρους. Παράλληλα, βελτίωνε το λιπιδαιμικό και γλυκαιμικό προφίλ, ενώ δεν είχε δυσμενή επίδραση σε αρτηριακή πίεση και καρδιακό ρυθμό. Βαλβιδοπάθειες παρατηρήθηκαν σε ποσοστό στατιστικά μη σημαντικό σε σχέση με το εικονικό φάρμακο.16,17 Οι ανεπιθύμητες ενέργειες της λορκασερίνης είναι κυρίως σεροτονινεργικές, όπως θάμβος όρασης, αϋπνία, ζάλη, ναυτία και γαστρεντερικές διαταραχές. Πρόκειται για δυνητικά τερατογόνο φάρμακο, για τον λόγο αυτό αντενδείκνυται η χρήση της κατά την κύηση.4 Προβληματισμό δημιουργεί το ενδεχόμενο του σεροτονινεργικού συνδρόμου που μπορεί να προκαλέσει η λορκασερίνη. Πρόκειται για σύνδρομο που προκαλείται από την υπερβολική σεροτονινεργική σηματοδότηση και είναι δυνητικά απειλητικό για τη ζωή. Εκδηλώνεται με αϋπνία, σύγχυση, παραισθησίες, υπομανία, κώμα, αλλά και με συμπτώματα από το αυτόνομο νευρικό σύστημα όπως υπερθερμία, υπέρταση, ταχυκαρδία, τρόμο, μυόκλονο και σπασμούς. Σε πειραματόζωα και σε δοσολογία 84 φορές μεγαλύτερη από αυτήν που χορηγείται στον άνθρωπο, η λορκασερίνη προκάλεσε πέραν των ανωτέρω ψυχιατρικών και νευρολογικών διαταραχών, όγκους μαστών και εγκεφάλου, καθώς και βαλβιδοπάθειες.5 Δεδομένης και της μικρής αποτελεσματικότητάς της στην απώλεια βάρους, η λορκασερίνη δεν πήρε έγκριση για κυκλοφορία στην Ευρώπη, ενώ στις ΗΠΑ έχει εγκριθεί από το 2012, με σοβαρούς περιορισμούς χρήσης. Ειδικά για το φόβο του σεροτονινεργικού συνδρόμου, αντενδείκνυται η συγχορήγηση με αντικαταθλιπτικά της κατηγορίας των SSRIs και MAOIs.5,8,14
Λιραγλουτίδη
Πολύ πρόσφατα προστέθηκε στη φαρέτρα της φαρμακευτικής αντιμετώπισης της παχυσαρκίας ένα φάρμακο που χρησιμοποιείται εδώ και αρκετά έτη στην αντιμετώπιση του διαβήτη τύπου 2. Πρόκειται για τη λιραγλουτίδη, ένα ανάλογο μιας ινκρετίνης ορμόνης, του γλυκαγονόμορφου πεπτιδίου-1 (Glucagon-like-peptide-1, GLP-1), το οποίο έχει αποδείξει την αποτελεσματικότητά του στην αντιμετώπιση της υπεργλυκαιμίας, ενώ ταυτόχρονα μειώνει το σωματικό βάρος στους διαβητικούς ασθενείς. Η ανορεξιογόνος επίδραση της λιραγλουτίδης ασκείται μέσω προβολών του στελέχους στον τοξοειδή πυρήνα του υποθαλάμου, όπου αναστέλλει τη σηματοδότηση των ορεξιογόνων και ευοδώνει εκείνη των ανορεξιογόνων νευροπεπτιδίων.18 Έχει άλλωστε αποδειχθεί πλέον ότι σημαντικό ρόλο στην απώλεια βάρους μετά από γαστρική παράκαμψη κατά Roux-en-Y, αλλά και στις συνακόλουθες ευμενείς καρδιαγγειακές επιδράσεις 19 παίζει η μεγάλη μετεγχειρητική αύξηση ανορεξιογόνων γαστρεντερικών ορμονών, με προεξάρχον το GLP-1.20 Η μελέτη SCALE χορήγησε λιραγλουτίδη σε παχύσαρκους ασθενείς σε δόση 3.0 mg, σαφώς υψηλότερη της μεγίστης των 1.8 mg που χρησιμοποιείται στο διαβήτη. Φάνηκε σημαντική απώλεια βάρους έναντι του εικονικού φαρμάκου, με αποτέλεσμα που διατηρείτο για 2 έτη. (Σχήμα 4) Παράλληλα, βελτιώθηκε το γλυκαιμικό και λιπιδαιμικό προφίλ, μειώθηκε η αρτηριακή πίεση, αλλά παρατηρήθηκε μικρή αύξηση της καρδιακής συχνότητας.21 Το τελευταίο εύρημα ήταν ήδη γνωστό από τη χρήση του φαρμάκου για την αντιμετώπιση του διαβήτη. Για τη διαλεύκανση της καρδιοαγγειακής ασφάλειας της λιραγλουτίδης βρίσκεται σε εξέλιξη η μεγάλη κλινική μελέτη LEADER.4 Συνηθέστερες ανεπιθύμητες ενέργειες της λιραγλουτίδης είναι η ναυτία και τάση για έμετο, που είναι δοσοεξαρτώμενες και συνήθως υποχωρούν μετά τις πρώτες ημέρες χορήγησης.4 Όσον αφορά τον προβληματισμό που επικρατεί σε σχέση με τα GLP-1 ανάλογα και την πιθανή αυξημένη συχνότητα παγκρεατίτιδας και καρκίνου του παγκρέατος, πρόσφατη ανάλυση των σχετικών δεδομένων από το FDA και την Αμερικανική και Ευρωπαϊκή Διαβητολογική Εταιρεία οδήγησε σε καθησυχαστική ανακοίνωση. Ωστόσο, η χορήγησή τους αντενδείκνυται σε ασθενείς με σύνδρομο MEN, καθώς και με οικογενειακό ιστορικό μυελοειδούς καρκίνου του θυρεοειδούς. Η χορήγηση λιραγλουτίδης με ένδειξη την παχυσαρκία έλαβε έγκριση από το FDA το Δεκέμβριο του 2014 και από τον Ευρωπαϊκό Οργανισμό Φαρμάκων τον Ιανουάριο του 2015.
Μέλλον:
Η έρευνα που στοχεύει στην εξέλιξη φαρμακευτικών παραγόντων κατά της παχυσαρκίας είναι εντατική και στρέφεται προς ποικίλους μηχανισμούς. (Πίνακας 1) Δοκιμάζονται φάρμακα που στοχεύουν στους μηχανισμούς του κεντρικού νευρικού συστήματος για τη σηματοδότηση της πείνας και του κορεσμού, καθώς και συνδυασμοί, ούτως ώστε να επιτευχθεί συνεργική δράση με λιγότερες ανεπιθύμητες ενέργειες. Παράλληλα, διερευνώνται παράγοντες που εμπλέκονται στην εντερική ορμονική δραστηριότητα, η οποία επηρεάζει την πρόσληψη τροφής. Επίσης, δοκιμάζονται φάρμακα που συνδυάζουν τους δύο ανωτέρω μηχανισμούς. Μια πρόσφατη στρατηγική αναπτύσσει μονοαμινικά πεπτίδια με πολλαπλούς στόχους.3,22
Κάποιες ουσίες έχουν ενδεχομένως περισσότερο ενδιαφέρον. Η σετιλιστάτη είναι ένας νέος αναστολέας των γαστρεντερικών λιπασών, που φαίνεται ότι έχει καλύτερο προφίλ ανεπιθύμητων ενεργειών από την ορλιστάτη. Προσφάτως έλαβε έγκριση για χρήση στην Ιαπωνία.22 Από τα κεντρικώς δρώντα φάρμακα που έχουν ενδιαφέρον είναι ο συνδυασμός βουπροπιόνης με το αντιεπιληπτικό ζονισαμίδη, που έδειξε αποτελεσματικότητα σε μελέτες φάσης ΙΙ και πρόκειται να δοκιμαστεί σε μελέτη φάσης ΙΙΙ.8,22 Επίσης, η τεσοφενσίνη, ένας αναστολέας επαναπρόσληψης σεροτονίνης, νοραδρεναλίνης και ντοπαμίνης, που ξεκίνησε να μελετάται για τις νόσους Alzheimer και Parkinson, φάνηκε να μειώνει σημαντικά το σωματικό βάρος Βρίσκεται σε εξέλιξη μελέτη φάσης ΙΙΙ σε παχύσαρκα άτομα, υπάρχουν όμως αρκετοί ενδοιασμοί όσον αφορά τις ενδεχόμενες ανεπιθύμητες ενέργειές της.23
Από τα φάρμακα που βασίζονται σε ορμόνες του γαστρεντερικού σωλήνα, σημαντικές προοπτικές φαίνεται ότι έχουν το πεπτίδιο τυροσίνη – τυροσίνη (PYY) και η οξυντομοντουλίνη. Το PYY παράγεται φυσιολογικά από τα L κύτταρα του εντέρου και επιδρά με ανορεξιογόνο τρόπο στον τοξοειδή υποθαλαμικό πυρήνα. Εκκρίνεται μεταγευματικά και κατ’ αναλογία με το θερμιδικό φορτίο του γεύματος.24 Η εξωγενής χορήγησή του οδήγησε σε σημαντική μείωση της πρόσληψης τροφής σε πειραματόζωα και εθελοντές. Όμως, μελέτη στην οποία χορηγήθηκε PYY ενδορρινικά, δεν ολοκληρώθηκε λόγω της υψηλής συχνότητας εμφάνισης έντονης ναυτίας που οδήγησε αρκετούς ασθενείς να αποχωρήσουν.25 Η οξυντομοντουλίνη, γνωστή παλαιότερα ως εντερογλυκαγόνη, εκκρίνεται επίσης από τα L κύτταρα του εντέρου, κατά τρόπο παρόμοιο με το PYY. Έχει δράση ινκρετίνης και μειώνει τη γαστρική έκκριση και κινητικότητα, καθυστερώντας την πέψη.18 Η πειραματική της χορήγηση σε υγιείς εθελοντές οδήγησε σε μείωση της πρόσληψης τροφής και αύξηση της ενεργειακής δαπάνης.26 Συνθετικό ανάλογο οξυντομοντουλίνης δοκιμάζεται σε μελέτη φάσης ΙΙ. Αναστολείς ενεργοποιήσεως της ορεξιογόνου γαστρικής ορμόνης γκρελίνης και υβριδικά ανάλογα περισσότερων της μίας γαστρεντερικών ορμονών που εμπλέκονται στο ενεργειακό ισοζύγιο ενδέχεται να αποτελέσουν θεραπευτικές επιλογές.
Συμπεράσματα:
Στο παρελθόν έχουν χρησιμοποιηθεί πολλοί φαρμακευτικοί παράγοντες για την αντιμετώπιση της παχυσαρκίας, οι οποίοι όμως έχουν εγκαταλειφθεί κυρίως λόγω των σοβαρών ανεπιθύμητων ενεργειών τους. Σήμερα, στη φαρμακευτική φαρέτρα του κλινικού ιατρού υπάρχει μόνο η ορλιστάτη, ενώ δύο νεότερα σκευάσματα έλαβαν έγκριση για χρήση στην Ευρώπη. Κυκλοφορούν στις ΗΠΑ δύο επιπλέον επιλογές, με σημαντικούς περιορισμούς χορήγησης και με ανησυχίες για ανεπιθύμητες ενέργειες που δεν επέτρεψαν, τουλάχιστον προς το παρόν, την έγκρισή τους στην Ευρώπη. Η εντατική έρευνα στον τομέα της φαρμακευτικής αντιμετώπισης της παχυσαρκίας ενδέχεται να καταλήξει σε νέους παράγοντες που επιδρούν τόσο στους κεντρικούς όσο και στους περιφερικούς μηχανισμούς που εμπλέκονται στη ρύθμιση του σωματικού βάρους, είτε μέσω μείωσης της πρόσληψης τροφής, ή αύξησης των ενεργειακών δαπανών.
Σχήματα:
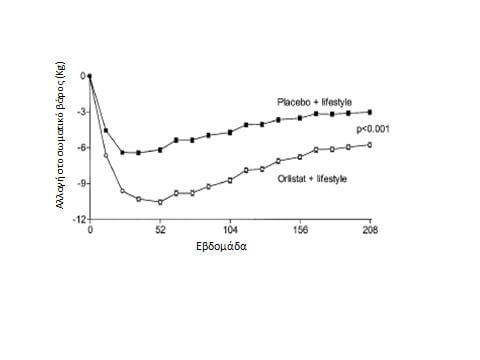
Σχήμα 1: Σύγκριση της ορλιστάτης με εικονικό φάρμακο στη μελέτη XENDOS. Προσαρμογή από Torgerson JS et al, Diabetes Care 2004;27:155-161
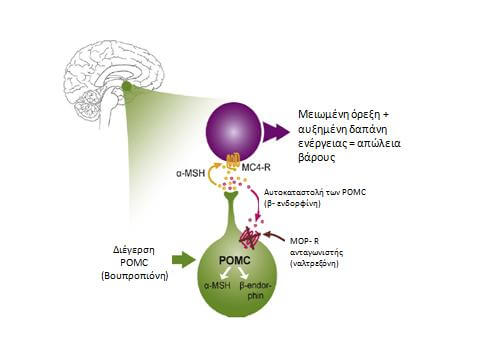
Εικόνα 1: Ο μηχανισμός δράσης του συνδυασμού βουπροπιόνης και ναλτρεξόνης στον υποθάλαμο. Προσαρμογή από Billes SK et al, Pharmacol Res 2014;84:1-11
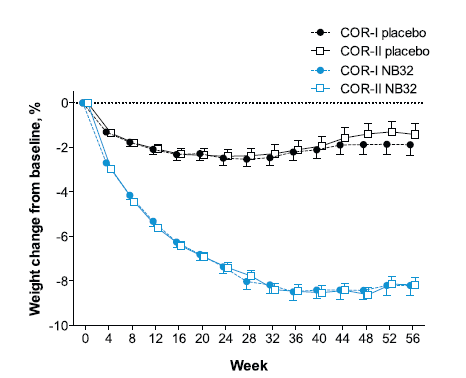
Σχήμα 2: Σύγκριση του συνδυασμού ναλτρεξόνης/βουπροπιόνης με εικονικό φάρμακο στις μελέτες COR-I και COR-II. Προσαρμογή από Billes SK et al, Pharmacol Res 2014;84:1-11
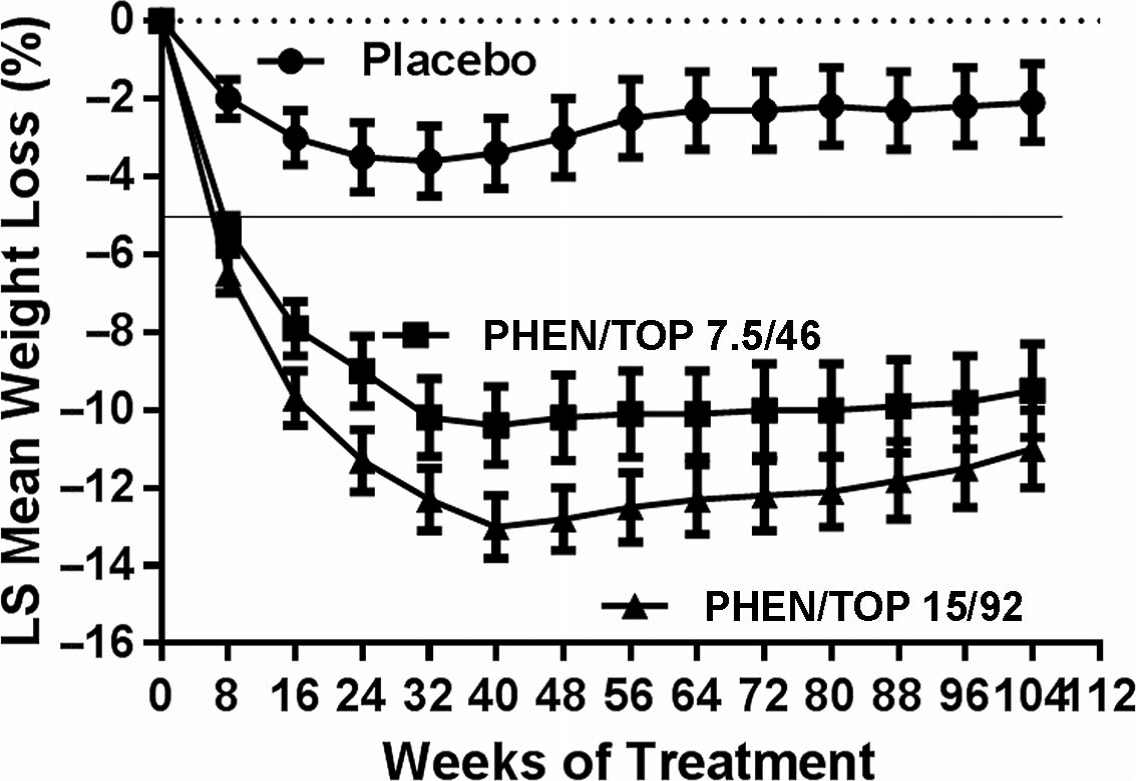
Σχήμα 3: Επίδραση του συνδυασμού φεντερμίνης/τοπιραμάτης στο σωματικό βάρος σε δύο διαφορετικές δοσολογίες (μελέτη CONQUER). Μετά τις 56 εβδομάδες δόθηκε η ευκαιρία στους ασθενείς να συνεχίσουν για ακόμη έναν χρόνο (μελέτη SEQUEL), με σημαντική διατήρηση της αποτελεσματικότητας. Προσαρμογή από Bray GA, Ryan DH, Ann NY Acad Sci 1311 (2014) 1 – 13.

Σχήμα 4: Η επίδραση της λιραγλουτίδης στο σωματικό βάρος στη μελέτη SCALE Maintenance. Προσαρμογή από Wadden TA et al, Int J Obes (Lond) 2013;37:1143-1151
| Φάρμακο | Μηχανισμός δράσης | Φάση κλινικής δοκιμής |
| Cetilistat | Αναστολέας παγκρεατικών λιπασών | Κυκλοφορεί στην Ιαπωνία |
| Contrave (bupropion/naltrexone) | Αναστολέας επαναπρόσληψης ντοπαμίνης και νοραδρεναλίνης/ αγωνιστής μ- υποδοχέων οπιοειδών | ΙΙΙ (τρέχουσα) |
| Empatic (zonisamide/ bupropion) | CA αναστολέας/ Αναστολέας επαναπρόσληψης ντοπαμίνης και νοραδρεναλίνης | ΙΙ (ολοκληρωμένη) |
| Liraglutide | GLP-1 ανάλογο μακράς δράσης | ΙΙΙ (τρέχουσα) |
| Velneperit | Ανταγωνιστής υποδοχέων Νευροπεπτιδίου Υ5 | ΙΙ (ολοκληρωμένη) |
| Tesofensine | Τριπλός αναστολέας επαναπρόσληψης μονοαμινών | ΙΙ (ολοκληρωμένη) |
| JNJ-16269110 | Αναστολέας MTP | ΙΙ (ολοκληρωμένη) |
| ΤΤΡ-436 | AgRP αναστολέας | ΙΙ (ολοκληρωμένη) |
| Beloranib | MetAP-2 αναστολέας | ΙΙ (τρέχουσα) |
| Oxyntomodulin | Διπλός αγωνιστής υποδοχέων GLP-1 και γλυκαγόνης | ΙΙ (τρέχουσα) |
| GSK 1521498 | Αντίστροφος αγωνιστής μ- οπιοειδών | Ι (ολοκληρωμένη) |
| GSK 598809 | Ανταγωνσιτής D3 ντοπαμίνης | Ι (ολοκληρωμένη) |
| PF-04971729 | Εκλεκτικός αναστολέας του εξαρτώμενου από το νάτριο συμμεταφορέα 2 της γλυκόζης | Ι (ολοκληρωμένη) |
| PF-04260110 | Εκλεκτικός αναστολέας DGAT-1 | Ι (ολοκληρωμένη) |
| AgRP: agouti-related protein, CA: carbonic anhydrase, DGAT-1: diglyceride acyl transferase 1, GLP-1: glucagon-like peptide 1, MetAP-2: methionine aminopeptidase 2, MTP: microsomal triglyceride transfer protein | ||
Πίνακας 1: Φαρμακευτικοί παράγοντες κατά της παχυσαρκίας σε φάση κλινικών μελετών. Προσαρμογή από George M et al, J Cardiovasc Pharmacol Ther 2014;19:65-76.
ΒΙΒΛΙΟΓΡΑΦΙΚΕΣ ΑΝΑΦΟΡΕΣ:
- WHO | Obesity and overweight. WHO. [cited 2014 Apr 14]. Available from: http:// who.int/mediacentre/factsheets/fs311/en/.
- Lim SS, Vos T, Flaxman AD, et al. A comparative risk assessment of burden of disease and injury attributable to 67 risk factors and risk factor clusters in 21 regions, 1990-2010: a systematic analysis for the Global Burden of Disease Study 2010. Lancet 2012;380:2224-22
- Kakkar AK, Dahiya N. Drug treatment of obesity: Current status and future prospects. Eur J Inter Med doi:10.1016/j.ejim.2015.01.005
- Pucci A, Finer N. New Medications for Treatment of Obesity: Metabolic and Cardiovascular Effects. Can J Cardiol 2015;31:142-152
- Bray GA. Medical treatment of obesity: The past, the present and the future. Best Pract Res Clin Gastroenterol 2014;28:665-684
- Ioannides-Demos LL, Proietto J, McNeil JJ. Pharmacotherapy for obesity. Drugs 2005;65:1391-1418
- Halford JC. Clinical pharmacotherapy for obesity: current drugs and those in advanced development. Curr Drug Targets 2004;5:637-646
- Heal DJ, Gosden J, Smith SL. A review of late-stage CNS drug candidates for the treatment of obesity. Int J Obes 2013;37:107-117
- Wierzbicki AS. Rimonabant: endocannabinoid inhibition for the metabolic syndrome. Int J Clin Pract 2006;60:1697-1706
- Torgerson JS Hauptman J, Boldrin MN et al. XENical in the prevention of diabetes in obese subjects (XENDOS) study: a randomized study of orlistat as an adjunct to lifestyle changes for the prevention of type 2 diabetes in obese patients. Diabetes Care 2004;27:155-161
- Billes SK, Sinnayah P, Cowley MA. Naltrexone/bupropion for obesity: An investigational combination pharmacotherapy for weight loss. Pharmacol Res 2014;84:1-11
- Greenway FL, Fujioka K, Plodkowski RA et al. Effect of naltrexone plus bupropion on weight loss in overweight and obese adults (COR-I): a multicentre, randomised, double-blind, placebo-controlled, phase 3 trial. Lancet 2010;376:595-605
- Bray GA, Ryan DH. Update on obesity pharmacotherapy. Ann NY Acad Sci 2014;1311:1–13
- Heal DJ, Gosden J, Smith SL. What is the prognosis for new centrally-acting anti-obesity drugs? 2012;63:132-146
- Taylor JR, Dietrich E, Powell JG. New and Emerging Pharmacologic Therapies for Type 2 Diabetes, Dyslipidemia, and Obesity. Clin Ther 2013;35:1-17
- Manning S, Pucci A, Finer N. Pharmacotherapy for obesity: novel agents and paradigms. Ther Adv Chronic Dis 2014;5:135-148
- Shyh G, Cheng-Lai A. New Antiobesity Agents Lorcaserin (Belviq) and Phentermine/Topiramate ER (Qsymia). Cardiology in Review 2013;22: 43–50.
- Kokkinos A, Alexiadou K, Liaskos C et al. Improvement in cardiovascular indices after Roux-en-Y gastric bypass or sleeve gastrectomy for morbid obesity. Obes Surg.2013;23:31-38
- Gardiner JV, Jayasena CN, Bloom SR. Gut hormones: a weight off your mind. J Neuroendocrinol.2008;20:834-841
- Le Roux CW, Welbourn R, Werling M et al. Gut hormones as mediators of appetite and weight loss after Roux-en-Y gastric bypass. Ann 2007;246:780-5
- Wadden TA, Hollander P, Klein S et al. Weight maintenance and additional weight loss with liraglutide after low-calorie-diet-induced weight loss: the SCALE Maintenance randomized study. Int J Obes (Lond) 2013;37:1143-1151
- George M, Rajaram M, Shanmugam Ε. New and Emerging Drug Molecules Against Obesity. J Cardiovasc Pharmacol Ther 2014;19:65-76
- Astrup A, Madsbad S, Breum L et al. Effect of tesofensine on bodyweight loss, body composition, and quality of life in obese patients: a randomised, double-blind, placebo-controlled trial. Lancet 2008;372:1906-1913
- Simpson KA, Bloom SR. Appetite and hedonism: gut hormones and the brain. Endocrinol Metab Clin North Am.2010;39:729-743
- Gantz I, Erondu N, Mallick M et al. Efficacy and safety of intranasal peptide YY3-36 for weight reduction in obese adults. J Clin Endocrinol Metab.2007;92:1754-1757
- Wynne K, Park AJ, Small CJ et al. Oxyntomodulin increases energy expenditure in addition to decreasing energy intake in overweight and obese humans: a randomised controlled trial. Int J Obes (Lond).2006 ;30:1729-1736

